Contaminación química
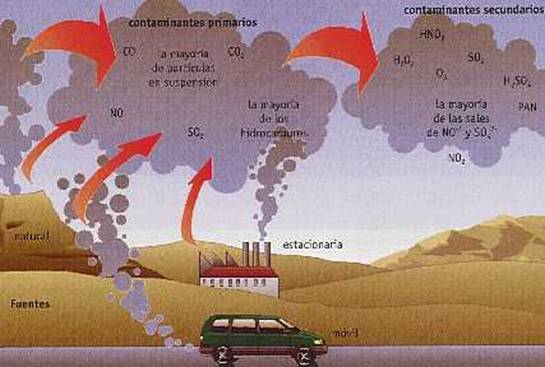
Suele estar producida por dos grandes grupos de contaminantes, primarios y secundarios
Contaminantes primarios
Llegan directamente desde las fuentes emisoras
- Partículas en suspensión: 0,1 - 25μ dispersas.
- Cenizas: volcánico, incendios, polvo, de combustiones.
- Líquidas: oleaje y óxidos
- Las más finas y los sulfatos son más perjudiciales: ataques de asma.
- Cubren las hojas,
- Cubren monumentos
 Contaminación en China
Contaminación en China
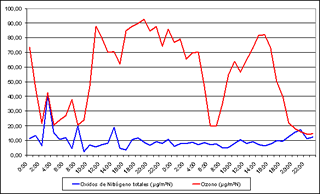
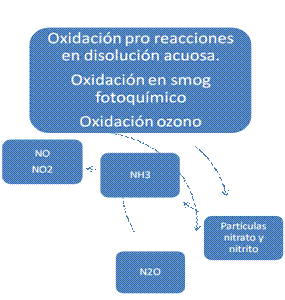
Óxidos de nitrógeno
Óxido nitroso N2O |
Desnitrificación bacteriana: uso de abonos. Incoloro |
Óxido Nítrico NO |
Desnitrificación, fijación cósmica, combustiones. Incoloro |
Dióxido de nitrógeno NO2 |
Combustiones. Pardo rojizo. |
|
|
Óxidos de azufre y sulfatos
- El dióxido de azufre (SO2) es el más contaminante: es un gas incoloro y no inflamable, más denso que aire , de olor acre e irritante.
- Procede de la producción energética y térmica que deriva del consumo de combustibles fósiles que contienen azufre. La mayor parte del azufre nocivo se forma durante el procesamiento del gas natural y en el refinamiento del petróleo.
- L a mitad proviene de combustión carbón y fuel e incendios. La otra, de volcanes, océanos y zonas pantanosas, donde anaeróbicamente se descompone, originando H2S, que se oxida a SO2
Ciclo azufre
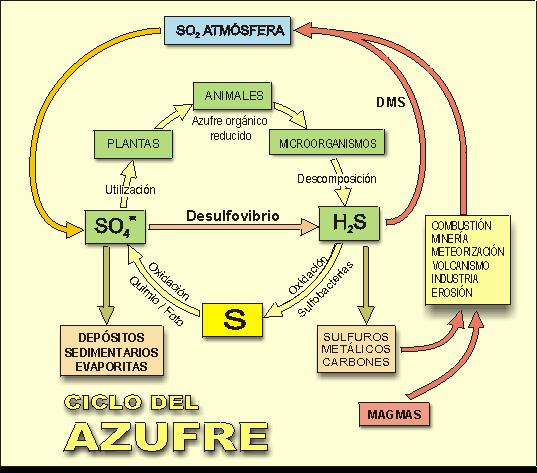
Azufre
|
|
|
|
Óxidos de Carbono
- Monóxido de carbono incoloro e inodoro: causamos 10% por combustión incompleta.
- Bloqueo de Hb
- CO2: aumenta 0,5% cada año
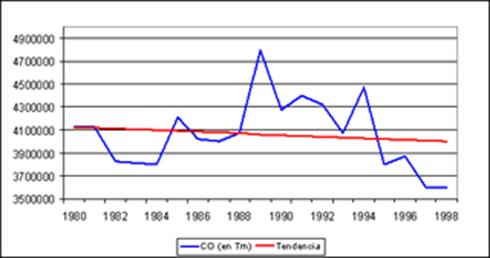
Gráfico 1.- Emisiones de monóxido de carbono en España entre 1980 y 1998, en millones de toneladas. Fuente, Ministerio de Medio Ambiente.
- CO2
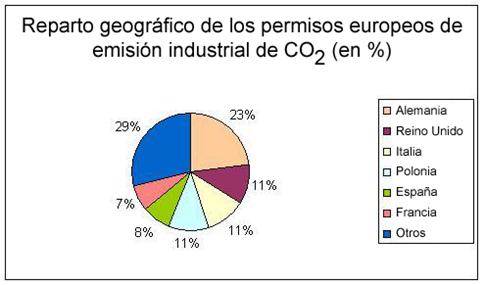
Hidrocarburos
- En principio son contaminantes primarios muy diversos, entre los que destaca el metano -CH4- , que forman posteriormente oxidantes fotoquímicos, con efectos más acusados y graves.
- De éstos, los más importantes parecen ser el ozono y los nitratos de peroxiacilo y de peroxibenzoílo.

Metano
- El ganado, las reacciones de putrefacción y la digestión de las termitas forma metano en grandes cantidades. También se desprende del gas natural, del que es un componente mayoritario y en algunas combustiones. Asimismo se forman grandes cantidades de metano en los procesos de origen humano hasta constituir, según algunos autores, cerca del 50% del emitido a la atmósfera.
- Desaparece de la atmósfera a consecuencia, principalmente, de reaccionar con los radicales OH formando, entre otros compuestos, ozono. Su vida media en la troposfera es de entre 5 y 10 años.
- Se considera que no produce daños en la salud ni en los seres vivos, pero influye de forma significativa en el efecto invernadero y también en las reacciones estratosféricas.
- En España la gran mayoría del metano emitido a la atmósfera procede de cuatro fuentes, en proporciones muy similares: la agricultura y ganadería, el tratamiento de residuos, el tratamiento y distribución de combustibles fósiles y las emisiones naturales que tienen lugar, sobre todo, en las zonas húmedas.
Metales pesados
Elemento |
Fuentes |
Efectos |
Berilio |
Carbón, industria |
Más tóxico, se acumula en pulmones: berilosis |
Cadmio |
Carbón, minería cinc, conducciones, tabaco |
Cardiovasculares, hipertensión. |
Plomo |
Escape coches |
Daños cerebrales. Saturnismo |
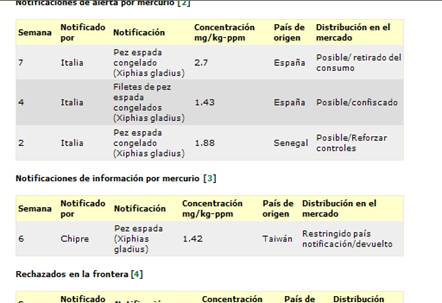
Mercurio |
Carbón, industria, aparatos eléctrico |
Daños en nervips u muerte |
Niquel |
Carburante Diese, petróleo, carbón, tabaco, químicos |
Carcinógeno. |
|
|
Compuestos halogenados
- Derivados de cloro, fluor.
- Los más peligrosos, los CFC, gases que al ser estables se usan en aerosoles y espumas e industrias del frío.
- Liberan cloro que ataca al ozono.
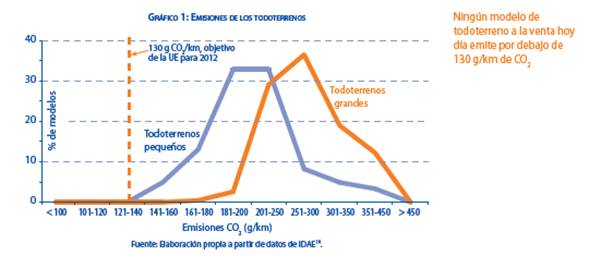
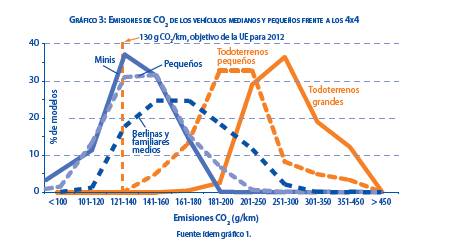
Diesel o gasolina
- ¿Diesel o gasolina?


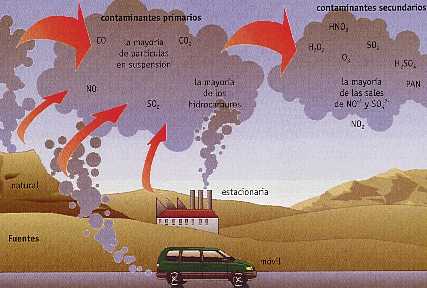
Contaminantes secundarios
- La energía de luz solar provoca en contaminantes primarios una serie de reacciones que los transforman en radicales altamente reactivos
Ozono
|
|
Ozono
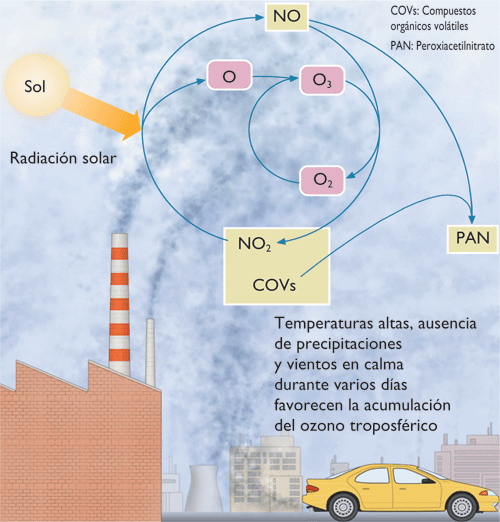
- Se forma por reacción entre otros gases contaminantes (óxidos de nitrógeno y compuestos orgánicos volátiles) con la participación de la radiación solar.
- Hay una cierta presencia natural de ozono troposférico, intrusiones del ozono estratosférico ,ocasionado por la reacción de los óxidos de nitrógeno naturales y determinados compuestos de origen vegetal.
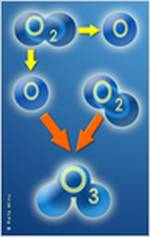
Ozono
- El ozono es una forma de oxígeno cuya molécula tiene tres átomos, en vez de los dos del oxígeno común. El tercer átomo es el que hace que el gas que respiramos sea venenoso; mortal, si se aspira una pequeñísima porción de esta sustancia. Por medio de procesos atmosféricos naturales, las moléculas de ozono se crean y se destruyen continuamente. Las radiaciones ultravioletas del sol descomponen las moléculas de oxígeno en átomos que entonces se combinan con otras moléculas de oxígeno para formar el ozono.

Otros
- Compuestos orgánicos volátiles: dioxinas y furanos
- Derivados de nitratos y sulfatos, que contribuyen a formación ozono.

Efectos supraindividuales
- La atmósfera transforma sus componentes debido a la energía fotoquímica que recibe del sol.
- Por ello, se integran los contaminantes:
- Características emisión, meteorológicas, topográficas, geográficas…
- Se clasifican por los efectos locales y regionales.
Efectos locales
- Islas térmicas: producen calor y contaminación.
- Frenan vientos suaves y los contaminantes no se dispersan ni depositan.
- Aire cálido asciende y al enfriarse desciende por la periferia: esta cúpula retiene la circulación y mantiene Tª superiro a zonas colindantes: es la isla térmica.
- La opacidad inhibe a la radiación
- Islas térmicas
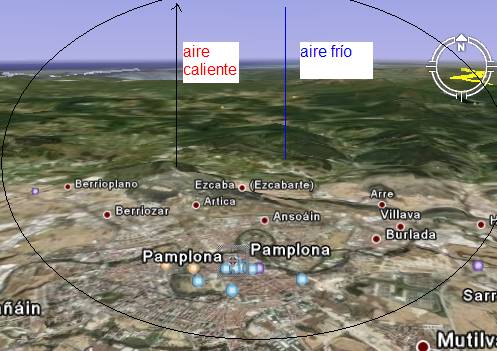
Variación precipitaciones
- Partículas
- Los contaminantes que no están en la atmósfera en forma de gas se llaman partículas. Pueden ser sólidas o líquidas.
- Las partículas contaminantes actúan como núcleos de condensación: las grandes, que tienen una concentración entre 10 y 15 veces superiores a normal
Smog
- Humo+ niebla: forman atmósferas muy húmedas y aire quieto que no dispersa.
- Ciudades costeras y contaminación
- Smog ácido, por SO2
- Smog fotoquímico cuando reaccionan con hidrocarburos
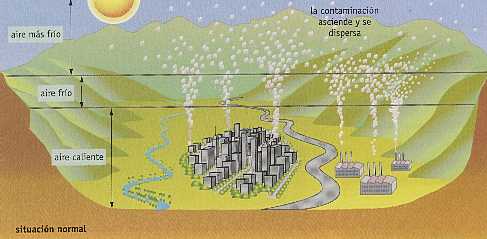
Lluvia ácida
Se denomina lluvia ácida a la caída a la superficie terrestre, mediante cualquier tipo de precipitación, de los ácidos disueltos en agua originados por contaminantes primarios, descargados a la atmósfera por determinadas actividades humanas, como el dióxido de azufre (SO2)y los óxidos de nitrógeno (NOx) al reaccionar en un proceso de transformación fotoquímica con determinados componentes atmosféricos (oxígeno, vapor de agua) durante su permanencia en la atmósfera.
|
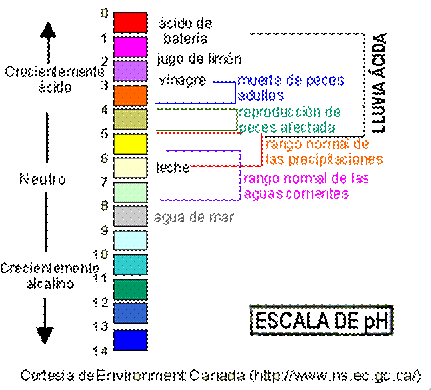
La lluvia ácida se identifica mediante la concentración de iones hidrógeno (H+) presentes en el medio (expresada como pH; pH = Log (concentración H+). |
Lluvia ácida
- Lo que hoy son actividades cotidianas, como:
- Emisiones industriales
- Gas de escape de los automóviles
- Emisiones urbanas (hogares)
- Liberan a la atmósfera SO2 y NOx
Lluvia ácida
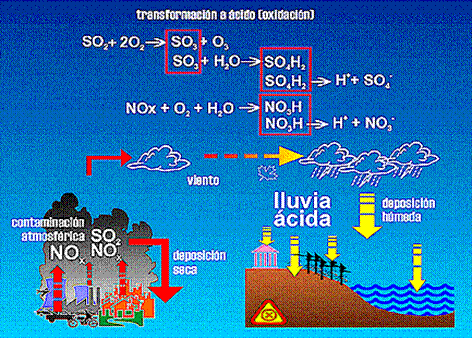
- Algunas de las moléculas que contaminan la atmósfera son ácidos o se convierten en ácidos con el agua de lluvia. El resultado es que en muchas zonas con grandes industrias se ha comprobado que la lluvia es más ácida que lo normal y que también se depositan partículas secas ácidas sobre la superficie, las plantas y los edificios. Esta lluvia ácida ya no es el don beneficioso que revitalizaría tierras, ríos y lagos; sino que, al contrario, trae la enfermedad y la decadencia para los seres vivos y los ecosistemas
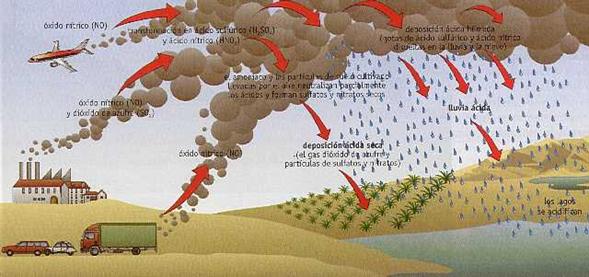
Causas
- Industrias o centrales térmicas que usan combustibles de baja calidad, liberan al aire importantes cantidades de óxidos de azufre y nitrógeno.
- Son trasladados a distancias de cientos de kilómetros , sobre todo cuando son emitidos a la atmósfera desde chimeneas muy altas.
- En la atmósfera los óxidos de nitrógeno y azufre son convertidos en ácido nítrico y sulfúrico que vuelven a la tierra con las precipitaciones de lluvia o nieve (lluvia ácida).
- Si no llueve, van cayendo partículas sólidas con moléculas de ácido adheridas (deposición seca).
- La lluvia normal es ligeramente ácida, por llevar ácido carbónico que se forma cuando el dióxido de carbono del aire se disuelve en el agua que cae. Su pH suele estar entre 5 y 6. Pero en las zonas con la atmósfera contaminada por estas sustancias acidificantes, la lluvia tiene valores de pH de hasta 4 o 3 y, en algunas zonas en que la niebla es ácida, el pH puede llegar a ser de 2,3, es decir similar al del zumo de limón o al del vinagre.
Daños ecosistemas acuáticos
- a) Ecosistemas acuáticos.-Fue precisamente observando la situación de cientos de lagos y ríos de Suecia y Noruega, entre los años 1960 y 1970, en los que se vio que el número de peces y anfibios iba disminuyendo de forma acelerada y alarmante, cuando se dio importancia a esta forma de contaminación.
- La reproducción de los animales acuáticos es alterada, hasta el punto de que muchas especies de peces y anfibios no pueden subsistir en aguas con pH inferiores a 5,5,.

Añadidos…
- Especialmente grave es el efecto en terrenos de roca no caliza, porque cuando el terreno es calcáreo, los iones alcalinos son abundantes en el suelo y neutralizan, en gran medida, la acidificación; pero si las rocas son granitos, o rocas ácidas pobres en cationes, los lagos y ríos se ven mucho más afectados por una deposición ácida que no puede ser neutralizada por la composición del suelo.
b) Ecosistemas terrestres.-
La influencia sobre las plantas y otros organismos terrestres no está tan clara, pero se sospecha que puede ser un factor muy importante de la llamada "muerte de los bosques" que afecta a grandes extensiones de superficies forestales en todo el mundo. También parece muy probable que afecte al ecosistema terrestre a través de los cambios que produce en los suelos, pero se necesita seguir estudiando estos temas para conocer mejor cuales pueden ser los efectos reales.
c) Edificios y construcciones.-
La corrosión de metales y construcciones es otro importante efecto dañino producido por la lluvia ácida. Muchos edificios y obras de arte situadas a la intemperie se están deteriorando decenas de veces más aprisa que lo que lo hacían antes de la industrialización y esto sucede por la contaminación atmosférica, especialmente por la deposición ácida.
Ejemplos
- De los 200 millones de toneladas de SO2 que anualmente se emiten a la atmósfera, aproximadamente un 50% son de origen humano, produciéndose la mayoría en las áreas industrializadas del Hemisferio Norte (un 5% de la superficie terrestre).
- En la UE la reducción de las emisiones de SO2 es positiva (un 12% menos en 1990, debiendo alcanzar una reducción del 35% en el año 2000) pero negativa con respecto a los NOx (un 7% más en 1990, muy alejado del objetivo de una reducción de emisiones del 30% para el año 2000).
Como ejemplo de emisión SO2
- Una fundición de cobre que emplee diariamente 2.250 toneladas de mineral concentrado al 30% de azufre puede emitir al día 1350 toneladas de SO2.
- Una refinería de petróleo puede expulsar al aire entre 400 y 500 toneladas de SO2 por día.
- En París y su periferia, en 1964, se emitieron a la atmósfera entre 48.000 y 60.000 toneladas de SO2 procedentes de la calefacción y de la pequeña industria (carbón con un 1% de azufre).
- De los 200 millones de toneladas de SO2 que anualmente se emiten a la atmósfera, aproximadamente un 50% son de origen humano, produciéndose la mayoría en las áreas industrializadas del Hemisferio Norte (un 5% de la superficie terrestre).
- En la UE la reducción de las emisiones de SO2 es positiva (un 12% menos en 1990, debiendo alcanzar una reducción del 35% en el año 2000) pero negativa con respecto a los NOx (un 7% más en 1990, muy alejado del objetivo de una reducción de emisiones del 30% para el año 2000).
Transporte
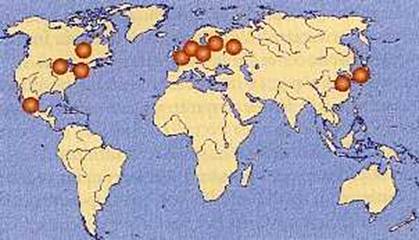 |
Transporte condicionado por circulación atmosférica y frenado por cationes, Na, K,Ca, Mg y amonio. |
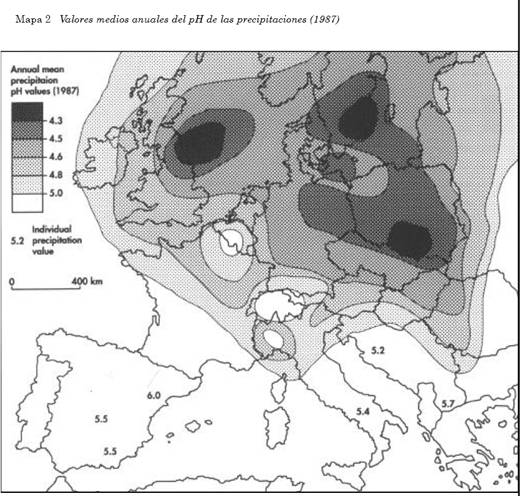
Bosque contaminado por lluvia ácida

Lluvia ácida
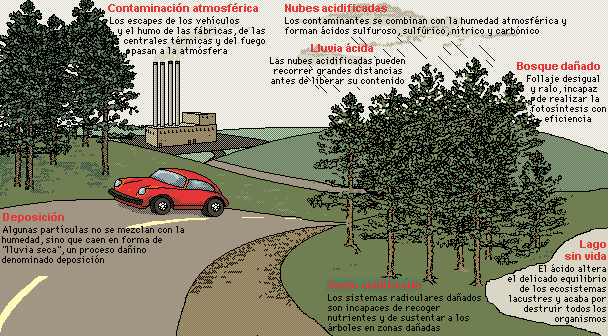
Noticias relacionadas

http://www.celfosc.org/news/000925.cnn.htm?=
http://news.bbc.co.uk/hi/spanish/science/newsid_5290000/5290588.stm


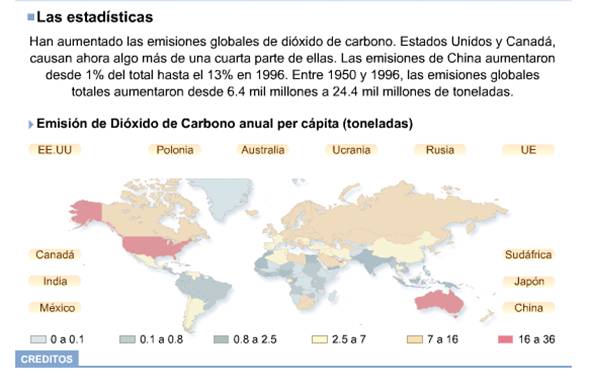
Actualizado en mayo de 2010