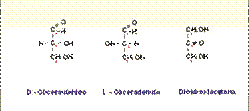MONOSACARIDOS
Definición
.-Son los más simples, a partir de los que se originan los demás y son la principal fuente de energía. Son blancos o incoloros, cristalinos, dulces y solubles en agua.
Están formados por una sola molécula de polihidroxicetona o polihidroxialdehido, con nº de C entre 3 y 9, unidos todos a grupos hidroxilo (-OH) formando alcoholes, salvo uno que está unido a un carbonilo (=O). Para nombrarlo se antepone a la terminación -osa un prefijo que indique si poseen la función aldehido o cetona y otro referente al número de C que posee la molécula.
El segundo C del Gliceraldehido tiene sus 4 valencias saturadas con 4 radicales diferentes: es un C asimétrico.
•Las hexosas , son glúcidos con 6 átomos de carbono. Entre ellas tienen interés en biología, la glucosa y galactosa entre las aldohexosas y la fructosa entre las cetohexosas.
Ciclación
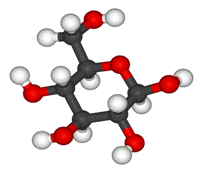
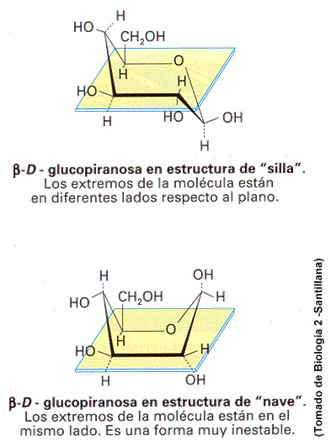
- Aldopentosas y hexosas en disolución, adoptan estructuras cíclicas de forma pentagonal o hexagonal
- Proyecciones de Haworth, con estructuras cíclicas en un plano y radicales en parte inferior y superior
-
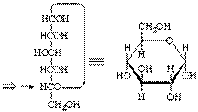 •Enlace hemiacetal: Enlace covalente entre gupo aldehído y alcohol•Enlace hemicetal: entre grupo cetona y alcohol•No implica pérdida ni ganancia de átomos•http://www.biorom.uma.es/contenido/biomodel/biomodel-misc/anim/gluc/glc.html•En disolución, se ciclan en anillos de lados, los furanos
•Enlace hemiacetal: Enlace covalente entre gupo aldehído y alcohol•Enlace hemicetal: entre grupo cetona y alcohol•No implica pérdida ni ganancia de átomos•http://www.biorom.uma.es/contenido/biomodel/biomodel-misc/anim/gluc/glc.html•En disolución, se ciclan en anillos de lados, los furanos•En disolución, se ciclan en anillos de 6 lados, los piranos
Normalmente se presentan en forma de cis o de trans
Isomería
Isomería geométrica o estereoisomería
-Configuración D y L, que son enantiomorfos, estereoisómeros ( los 4 radicales se pueden disponer según dos configuraciones distintas, no superponibles) uno imagen especular del otro.
En la naturaleza predominan los D. Las dos tienen las mismas propiedades fisica y químicas, excepto que en disolución una de ellas desvía el plano de la luz polarizada a la dcha. , por lo que se denomina dextrógira (+) y el otro a la izquierda, por lo que se le denomina levógiro (-).Las moléculas que cumplen esto se denominan enantiómeros o isómeros ópticos. NO SE PUEDE IDENTIFICAR D CON DEXTROGIRO NI L CON LEVOGIRO. La DHA no tiene C asimétrico y no presenta actividad óptica.
Propiedades
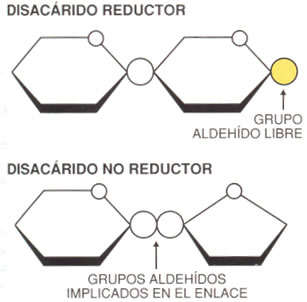
CARACTER REDUCTOR.-La presencia del grupo carbonílico les confiere la propiedad de ser reductores frente a ddas sustancias como el licor de Fehling, es decir, estas molécula se oxidan a ácido, reduciendo, por tanto, a ciertos iones metálicos, principalmente cobre o plata En medio alcalino reducen al ión cúprico, de color azul, a cuproso, precipitado Cu2O rojo ladrillo. SO4 Cu + NaOH -------Cu (OH)2
ACTIVIDAD ÓPTICA
La presencia de Carbonos asimétricos determina que los monosacáridos en disolución
tengan actividad óptica:
Desvían el plano de luz polarizada hacia la derecha o izquierda
-Cuando la rotación se produce en el sentido de las agujas del reloj: dextrógiras(+)
-Si es al contrario, levógiras o (-)
No se corresponde con forma D o L, no se distinguen a simple vista
Importancia biológica
Las triosas , son metabolitos intermediarios de la degradación de la glucosa |
|
Las pentosas, 5 C |
|
Las hexosas , |
|
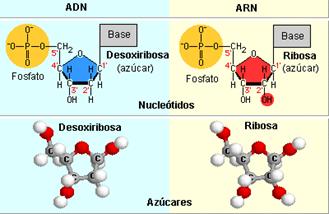
- Fosfatos de monosacáridos
- Desoxiazúcares
- Polialcoholes: Mioinositol
- Azucares ácidos
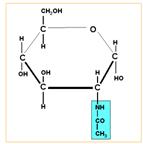
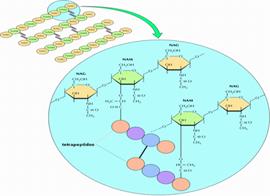
N-acetilglucosamina en la quitina de artrópodos |
|
N-acetilmurámico. En la pared celular de bacterias |
|